1. Ваше Имя и Фамилия: Alex Miroshnik
2. Должность: Зав.Отделением
3. Ксерокопия личного дела (( /time +/stats )) : Ксерокопия
4. Тема дипломной работы: Белки. Их роль в организме
Белки́ (
протеи́ны,
полипепти́ды) — высокомолекулярные органические вещества, состоящие из альфа-аминокислот, соединённых в цепочку пептидной связью. В живых организмах аминокислотный состав белков определяется генетическим кодом, при синтезе в большинстве случаев используется 20 стандартных аминокислот. Множество их комбинаций создают молекулы белков с большим разнообразием свойств. Кроме того, аминокислотные остатки в составе белка часто подвергаются посттрансляционным модификациям, которые могут возникать и до того, как белок начинает выполнять свою функцию, и во время его «работы» в клетке. Часто в живых организмах несколько молекул разных белков образуют сложные комплексы, например фотосинтетический комплекс.

Кристаллы различных белков, выращенные на космической станции «Мир» и во время полётов шаттлов НАСА. Высокоочищенные белки при низкой температуре образуют кристаллы, которые используют для изучения пространственных структур этих белков.
Функции белков в клетках живых организмов более разнообразны, чем функции других биополимеров — полисахаридов и ДНК. Так, белки-ферменты катализируют протекание биохимических реакций и играют важную роль в обмене веществ. Некоторые белки выполняют структурную или механическую функцию, образуя цитоскелет, поддерживающий форму клеток. Также белки играют ключевую роль в сигнальных системах клеток, при иммунном ответе и в клеточном цикле.
Белки — важная часть питания животных и человека (основные источники: мясо, птица, рыба, молоко, орехи, бобовые, зерновые; в меньшей степени: овощи, фрукты, ягоды и грибы), поскольку в их организмах не могут синтезироваться все незаменимые аминокислоты и часть должна поступать с белковой пищей. В процессе пищеварения ферменты разрушают потреблённые белки до аминокислот, которые используются для биосинтеза собственных белков организма или подвергаются дальнейшему распаду для получения энергии.
Определение аминокислотной последовательности первого белка — инсулина — методом секвенирования белков принесло Фредерику Сенгеру Нобелевскую премию по химии в 1958 году. Первые трёхмерные структуры белков гемоглобина и миоглобина были получены методом дифракции рентгеновских лучей, соответственно, Максом Перуцем и Джоном Кендрю в конце 1950-х годов, за что в 1962 году они получили Нобелевскую премию по химии.
Роль белка в организме
Так же как и другие биологические макромолекулы (полисахариды, липиды и нуклеиновые кислоты), белки являются необходимыми компонентами всех живых организмов и играют важную роль в жизнедеятельности клетки. Белки осуществляют процессы обмена веществ. Они входят в состав внутриклеточных структур — органелл и цитоскелета, секретируются во внеклеточное пространство, где могут выступать в качестве сигнала, передаваемого между клетками, участвовать в гидролизе пищи и образовании межклеточного вещества.
Классификация белков по их функциям является достаточно условной, так как один и тот же белок может выполнять несколько функций. Хорошо изученным примером такой многофункциональности служит лизил-тРНК-синтетаза — фермент из класса аминоацил-тРНК-синтетаз, которая не только присоединяет остаток лизина к тРНК, но и регулирует транскрипцию нескольких генов. Многие функции белки выполняют благодаря своей ферментативной активности. Так, ферментами являются двигательный белок миозин, регуляторные белки протеинкиназы, транспортный белок натрий-калиевая аденозинтрифосфатаза и др.

Молекулярная модель фермента-
уреазы бактерии
Helicobacter pylori
Каталитическая функция
Наиболее хорошо известная функция белков в организме — катализ различных химических реакций. Ферменты — это белки, обладающие специфическими каталитическими свойствами, то есть каждый фермент катализирует одну или несколько сходных реакций. Ферменты катализируют реакции расщепления сложных молекул (катаболизм) и их синтеза (анаболизм), в том числе репликацию и репарацию ДНК и матричный синтез РНК. К 2013 году было описано более 5000 ферментов. Ускорение реакции в результате ферментативного катализа может быть огромным: реакция, катализируемая ферментом оротидин-5'-фосфатдекарбоксилазой, например, протекает в 10¹⁷ раз быстрее некатализируемой (период полуреакции декарбоксилирования оротовой кислоты составляет 78 миллионов лет без фермента и 18 миллисекунд с участием фермента). Молекулы, которые присоединяются к ферменту и изменяются в результате реакции, называются субстратами.
Хотя ферменты обычно состоят из сотен аминокислотных остатков, только небольшая часть из них взаимодействует с субстратом, и ещё меньшее количество — в среднем 3—4 аминокислотных остатка, часто расположенные далеко друг от друга в первичной структуре — напрямую участвуют в катализе. Часть молекулы фермента, которая обеспечивает связывание субстрата и катализ, называется активным центром.
Международный союз биохимии и молекулярной биологии в 1992 году предложил окончательный вариант иерархической номенклатуры ферментов, основанной на типе катализируемых ими реакции. Согласно этой номенклатуре названия ферментов всегда должны иметь окончание -
аза и образовываться от названий катализируемых реакций и их субстратов. Каждому ферменту приписывается индивидуальный код, по которому легко определить его положение в иерархии ферментов. По типу катализируемых реакций все ферменты делят на 6 классов:
- КФ 1: Оксидоредуктазы, катализирующие окислительно-восстановительные реакции;
- КФ 2: Трансферазы, катализирующие перенос химических групп с одной молекулы субстрата на другую;
- КФ 3: Гидролазы, катализирующие гидролиз химических связей;
- КФ 4: Лиазы, катализирующие разрыв химических связей без гидролиза с образованием двойной связи в одном из продуктов;
- КФ 5: Изомеразы, катализирующие структурные или геометрические изменения в молекуле субстрата;
- КФ 6: Лигазы, катализирующие образование химических связей между субстратами за счёт гидролиза дифосфатной связи АТФ или сходного трифосфата.
Структурная функция
Структурные белки цитоскелета, как своего рода арматура, придают форму клеткам и многим органоидам и участвуют в изменении формы клеток. Большинство структурных белков являются филаментозными: мономеры актина и тубулина это, например, глобулярные, растворимые белки, но после полимеризации они формируют длинные нити, из которых состоит цитоскелет, позволяющий клетке поддерживать форму. Коллаген и эластин — основные компоненты межклеточного вещества соединительной ткани (например, хряща), а из другого структурного белка кератина состоят волосы, ногти, перья птиц и некоторые раковины.

Fab-фрагмент мышиного антитела в комплексе с антигеном (вверху)
Защитная функция
Существует несколько видов защитных функций белков:
- Физическая защита. Физическую защиту организма обеспечивают коллаген — белок, образующий основу межклеточного вещества соединительных тканей (в том числе костей, хряща, сухожилий и глубоких слоёв кожи (дермы)); кератин, составляющий основу роговых щитков, волос, перьев, рогов и др. производных эпидермиса. Обычно такие белки рассматривают как белки со структурной функцией. Примерами белков этой группы служат фибриногены и тромбины, участвующие в свёртывании крови.
- Химическая защита. Связывание токсинов белковыми молекулами может обеспечивать их детоксикацию. Особенно важную роль в детоксикации у человека играют ферменты печени, расщепляющие яды или переводящие их в растворимую форму, что способствует их быстрому выведению из организма.
- Иммунная защита. Белки, входящие в состав крови и других биологических жидкостей, участвуют в защитном ответе организма как на повреждение, так и на атаку патогенов. Белки системы комплемента и антитела (иммуноглобулины) относятся к белкам второй группы; они нейтрализуют бактерии, вирусы или чужеродные белки. Антитела, входящие в состав адаптивной иммунной системы, присоединяются к чужеродным для данного организма веществам, антигенам, и тем самым нейтрализуют их, направляя к местам уничтожения. Антитела могут секретироваться в межклеточное пространство или закрепляться в мембранах специализированных В-лимфоцитов, которые называются плазмоцитами.
Регуляторная функция
Многие процессы внутри клеток регулируются белковыми молекулами, которые не служат ни источником энергии, ни строительным материалом для клетки. Эти белки регулируют продвижение клетки по клеточному циклу, транскрипцию, трансляцию, сплайсинг, активность других белков и многие другие процессы. Регуляторную функцию белки осуществляют либо за счёт ферментативной активности (например, протеинкиназы), либо за счёт специфичного связывания с другими молекулами. Так, факторы транскрипции, белки-активаторы и белки-репрессоры, могут регулировать интенсивность транскрипции генов, связываясь с их регуляторными последовательностями. На уровне трансляции считывание многих мРНК также регулируется присоединением белковых факторов.
Важнейшую роль в регуляции внутриклеточных процессов играют протеинкиназы и протеинфосфатазы — ферменты, которые активируют или подавляют активность других белков путём присоединения к ним или отщепления фосфатных групп.

Структура миоглобина
Сигнальная функция
Сигнальная функция белков — способность белков служить сигнальными веществами, передавая сигналы между клетками, тканями, о́рганами и организмами. Часто сигнальную функцию объединяют с регуляторной, так как многие внутриклеточные регуляторные белки тоже осуществляют передачу сигналов.
Сигнальную функцию выполняют белки-гормоны, цитокины, факторы роста и др.
Гормоны переносятся кровью. Большинство гормонов животных — это белки или пептиды. Связывание гормона с его рецептором является сигналом, запускающим ответную реакцию клетки. Гормоны регулируют концентрации веществ в крови и клетках, рост, размножение и другие процессы. Примером таких белков служит инсулин, который регулирует концентрацию глюкозы в крови.
Клетки взаимодействуют друг с другом с помощью сигнальных белков, передаваемых через межклеточное вещество. К таким белкам относятся, например, цитокины и факторы роста.
Цитокины — пептидные сигнальные молекулы. Они регулируют взаимодействия между клетками, определяют их выживаемость, стимулируют или подавляют рост, дифференцировку, функциональную активность и апоптоз, обеспечивают согласованность действий иммунной, эндокринной и нервной систем. Примером цитокинов может служить фактор некроза опухоли, который передаёт сигналы воспаления между клетками организма.
Транспортная функция
Молекулярная модель кальциевого канала, вид сверху
Растворимые белки, участвующие в транспорте малых молекул, должны иметь высокое сродство (аффинность) к субстрату, когда он присутствует в высокой концентрации, и легко его высвобождать в местах низкой концентрации субстрата. Примером транспортных белков можно назвать гемоглобин, который переносит кислород из лёгких к остальным тканям и углекислый газ от тканей к лёгким, а также гомологичные ему белки, найденные во всех царствах живых организмов.
Некоторые мембранные белки участвуют в транспорте малых молекул через мембрану клетки, изменяя её проницаемость. Липидный компонент мембраны водонепроницаем (гидрофобен), что предотвращает диффузию полярных или заряженных (ионы) молекул. Мембранные транспортные белки принято подразделять на белки-каналы и белки-переносчики. Белки-каналы содержат внутренние заполненные водой поры, которые позволяют ионам (через ионные каналы) или молекулам воды (через белки-аквапорины) перемещаться через мембрану. Многие ионные каналы специализируются на транспорте только одного иона; так, калиевые и натриевые каналы часто различают эти сходные ионы и пропускают только один из них. Белки-переносчики связывают, подобно ферментам, каждую переносимую молекулу или ион и, в отличие от каналов, могут осуществлять активный транспорт с использованием энергии АТФ. «Электростанция клетки» — АТФ-синтаза, которая осуществляет синтез АТФ за счёт протонного градиента, также может быть отнесена к мембранным транспортным белкам.
Запасная (резервная) функция
К таким белкам относятся так называемые резервные белки, которые запасаются в качестве источника энергии и вещества в семенах растений (например, глобулины 7S и 11S) и яйцеклетках животных. Ряд других белков используется в организме в качестве источника аминокислот, которые в свою очередь являются предшественниками биологически активных веществ, регулирующих процессы метаболизма.
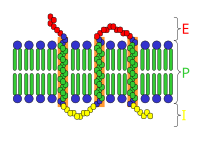
Схема трансмембранного рецептора: E — внеклеточное пространство; P — клеточная мембрана; I — внутриклеточное пространство
Рецепторная функция
Белковые рецепторы могут находиться как в цитоплазме, так и встраиваться в клеточную мембрану. Одна часть молекулы рецептора воспринимает сигнал, которым чаще всего служит химическое вещество, а в некоторых случаях — свет, механическое воздействие (например, растяжение) и другие стимулы. При воздействии сигнала на определённый участок молекулы — белок-рецептор — происходят её конформационные изменения. В результате меняется конформация другой части молекулы, осуществляющей передачу сигнала на другие клеточные компоненты. Существует несколько механизмов передачи сигнала. Некоторые рецепторы катализируют определённую химическую реакцию; другие служат ионными каналами, которые при действии сигнала открываются или закрываются; третьи специфически связывают внутриклеточные молекулы-посредники. У мембранных рецепторов часть молекулы, связывающаяся с сигнальной молекулой, находится на поверхности клетки, а домен, передающий сигнал, — внутри.
Моторная (двигательная) функция

Миозин — моторный белок
Целый класс моторных белков обеспечивает движения организма, например, сокращение мышц, в том числе локомоцию (миозин), перемещение клеток внутри организма (например, амебоидное движение лейкоцитов), движение ресничек и жгутиков, а также активный и направленный внутриклеточный транспорт (кинезин, динеин). Динеины и кинезины проводят транспортировку молекул вдоль микротрубочек с использованием гидролиза АТФ в качестве источника энергии. Динеины переносят молекулы и органоиды из периферических частей клетки по направлению к центросоме, кинезины — в противоположном направлении. Динеины также отвечают за движение ресничек и жгутиков эукариот. Цитоплазматические варианты миозина могут принимать участие в транспорте молекул и органоидов по микрофиламентам.
Белки в обмене веществ
Большинство микроорганизмов и растений могут синтезировать 20 стандартных аминокислот, а также дополнительные (нестандартные) аминокислоты, например, цитруллин. Но если аминокислоты есть в окружающей среде, даже микроорганизмы сохраняют энергию путём транспорта аминокислот внутрь клеток и выключения их биосинтетических путей.
Аминокислоты, которые не могут быть синтезированы животными, называются незаменимыми. Основные ферменты в биосинтетических путях, например, аспартаткиназа, которая катализирует первый этап в образовании лизина, метионина и треонина из аспартата, отсутствуют у животных.
Животные, в основном, получают аминокислоты из белков, содержащихся в пище. Белки разрушаются в процессе пищеварения, который обычно начинается с денатурации белка путём помещения его в кислотную среду и гидролиза с помощью ферментов, называемых протеазами. Некоторые аминокислоты, полученные в результате пищеварения, используются для синтеза белков организма, а остальные превращаются в глюкозу в процессе глюконеогенеза или используются в цикле Кребса. Использование белка в качестве источника энергии особенно важно в условиях голодания, когда собственные белки организма, в особенности мускулов, служат источником энергии. Аминокислоты также являются важным источником азота в питании организма.
Единых норм потребления белков человеком нет. Микрофлора толстого кишечника синтезирует аминокислоты, которые не учитываются при составлении белковых норм.
6. Дата: 30.06.20
7. Подпись: хХх









